- 153.50 KB
- 2022-05-14 15:46:54 发布
- 1、本文档共5页,可阅读全部内容。
- 2、本文档内容版权归属内容提供方,所产生的收益全部归内容提供方所有。如果您对本文有版权争议,可选择认领,认领后既往收益都归您。
- 3、本文档由用户上传,本站不保证质量和数量令人满意,可能有诸多瑕疵,付费之前,请仔细先通过免费阅读内容等途径辨别内容交易风险。如存在严重挂羊头卖狗肉之情形,可联系本站下载客服投诉处理。
- 文档侵权举报电话:19940600175。
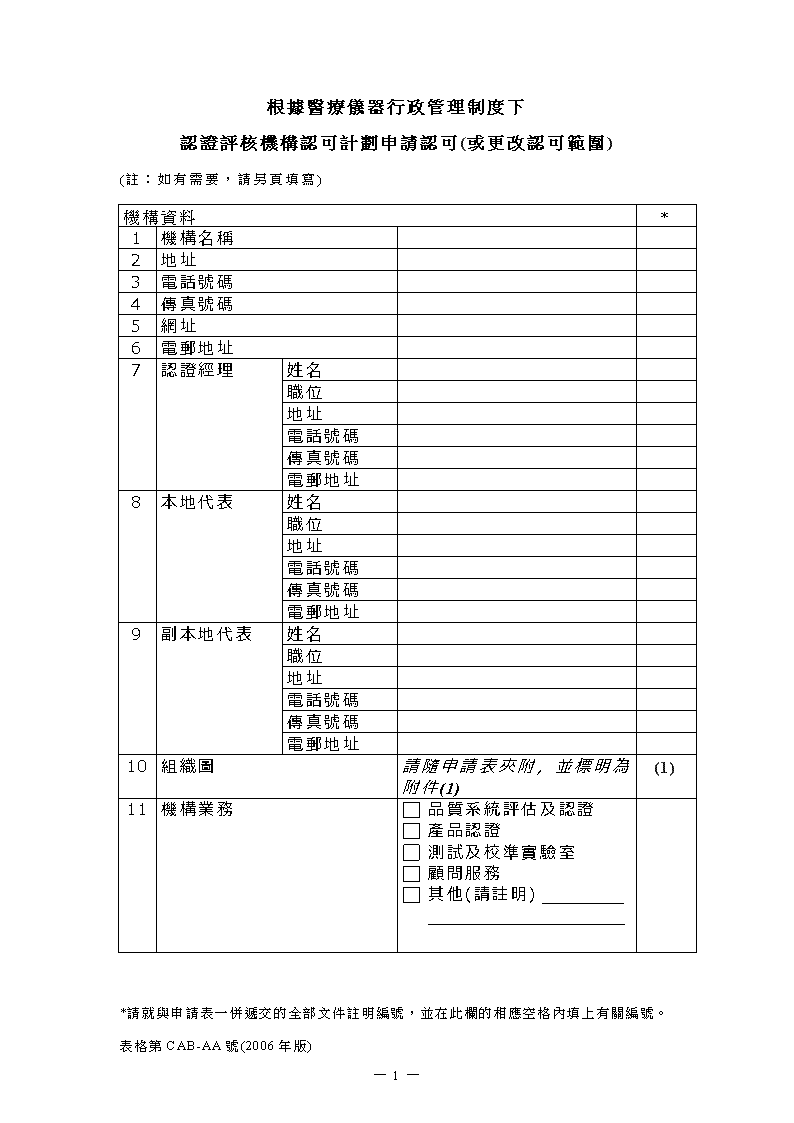
根據醫療儀器行政管理制度下認證評核機構認可計劃申請認可(或更改認可範圍)(註:如有需要,請另頁填寫)機構資料*1機構名稱2地址3電話號碼4傳真號碼5網址6電郵地址7認證經理姓名職位地址電話號碼傳真號碼電郵地址8本地代表姓名職位地址電話號碼傳真號碼電郵地址9副本地代表姓名職位地址電話號碼傳真號碼電郵地址10組織圖請隨申請表夾附,並標明為附件(1)(1)11機構業務品質系統評估及認證產品認證測試及校準實驗室顧問服務其他(請註明)*請就與申請表一併遞交的全部文件註明編號,並在此欄的相應空格內填上有關編號。表格第CAB-AA號(2006年版)-4-
12機構狀況(例如法人團體),另請提供可識別機構狀況的文件。13僱員數目14香港境外的辦事處地址15貴機構是否已在其他國家的規管制度(或任何其他制度,例如國際認可論壇(IAF)屬下成員對品質管理系統認機構的認可制度)下獲指定或獲認可為醫療儀器範疇或其相關範疇(例如電磁相容性)的認證評核機構?如是,請提供詳情(包括獲指定或獲認可的認證評核範圍)及證明文件。16貴機構如隸屬另一更大機構,請提供該更大機構及其架構的有關資料,特別是與貴機構的關係。申請認可的範圍*17申請以下述為限的(經修訂)範圍:(請說明申請認可的範圍是否包括型號檢驗。)產品範圍機構資源*18測試設施。請說明設施的所在地點及測試能力,並提供任何認證資格的詳情(包括證明文件)。*請就與申請表一併遞交的全部文件註明編號,並在此欄的相應空格內填上有關編號。表格第CAB-AA號(2006年版)-4-
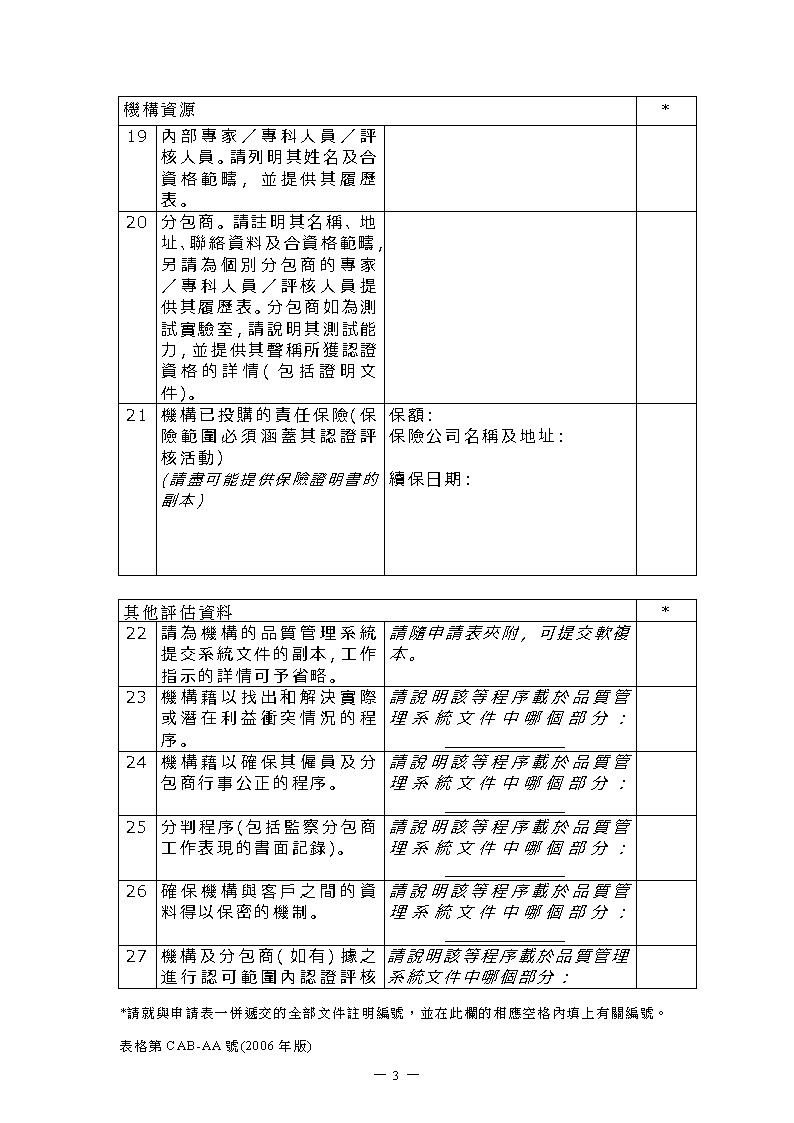
19內部專家/專科人員/評核人員。請列明其姓名及合資格範疇,並提供其履歷表。20分包商。請註明其名稱、地址、聯絡資料及合資格範疇,另請為個別分包商的專家/專科人員/評核人員提供其履歷表。分包商如為測試實驗室,請說明其測試能力,並提供其聲稱所獲認證資格的詳情(包括證明文件)。21機構已投購的責任保險(保險範圍必須涵蓋其認證評核活動)(請盡可能提供保險證明書的副本)保額:保險公司名稱及地址:續保日期:其他評估資料*22請為機構的品質管理系統提交系統文件的副本,工作指示的詳情可予省略。請隨申請表夾附,可提交軟複本。23機構藉以找出和解決實際或潛在利益衝突情況的程序。請說明該等程序載於品質管理系統文件中哪個部分:____________24機構藉以確保其僱員及分包商行事公正的程序。請說明該等程序載於品質管理系統文件中哪個部分:____________25分判程序(包括監察分包商工作表現的書面記錄)。請說明該等程序載於品質管理系統文件中哪個部分:____________26確保機構與客戶之間的資料得以保密的機制。請說明該等程序載於品質管理系統文件中哪個部分:____________27機構及分包商請說明該等程序載於品質管理系統文件中哪個部分:*請就與申請表一併遞交的全部文件註明編號,並在此欄的相應空格內填上有關編號。表格第CAB-AA號(2006年版)-4-
(如有)據之進行認可範圍內認證評核的程序____________28機構與分包商所訂協議的樣本。如有,請隨申請表夾附。*請就與申請表一併遞交的全部文件註明編號,並在此欄的相應空格內填上有關編號。表格第CAB-AA號(2006年版)-4-
申請人須知1.在本須知及下述聲明內:(i)「醫療儀器行政管理制度」意指MedicalDeviceAdministrativeControlSystem,縮寫為MDACS;(ii)「醫療儀器管制辦公室」意指MedicalDeviceControlOffice,縮寫為MDCO;(iii)「認證評核機構認可計劃」或「認可計劃」意指醫療儀器行政管理制度下的「認證評核機構認可計劃」;(iv)「政府」意指香港特別行政區政府。2.認證評核機構認可計劃的現行規定,可從本表格及醫療儀器管制辦公室所編製的其他公開文件(包括但不限於指南第GN-04號)得到確定。3.指南第GN-04號內所述的認證評核機構認可事宜上訴委員會,由沒有直接參與認證評核機構認可計劃管理工作的政府官員組成。表格第CAB-AA號(2006年版)-8-
4.醫療儀器管制辦公室就醫療儀器行政管理制度的執行或管理並特別就本申請而向申請人或其他人士所取得的保密資料(包括個人資料),將由政府及其內部門基於執行或管理該制度的目的而保留、處理和使用。此外,政府只會在下列情況將有關資料用於其他用途或向其他人士披露:(i)得到原先提供該保密資料人士的同意;或(ii)香港特別行政區的法例有所規定;或(iii)合乎公眾利益和法例規定。5.包括認證評核機構認可計劃在內的醫療儀器行政管理制度,只擬作為實施較長遠法定規管制度的前期安排,而非永久安排。政府在籌劃該較長遠的規管制度時,將在適當時考慮實施醫療儀器行政管理制度所得的經驗,但政府並無就醫療儀器行政管理制度的規定與較長遠規管制度的規定之間的異同作出任何陳述或保證。該較長遠的規管制度只會在其據之設立的法例通過後予以實施。表格第CAB-AA號(2006年版)-8-
聲明(簽署本聲明前請參閱申請人須知)1.本公司(申請人名稱及地址)謹此聲明:(i)本申請表及任何補充附頁所提供的資料均屬真確無誤;及(ii)與本申請表一併遞交的文件均為正本或真確副本。2.我們明白並同意,認證評核機構認可計劃的規定將會不時修訂。我們明白,醫療儀器管制辦公室會就更新後的規定以書面方式通知我們及/或藉其編製的公開文件(例如指南第GN-04號修訂版)向外公布。我們承諾遵守認可計劃的最新規定,也會遵守生署或醫療儀器管制辦公室根據認可計劃所作任何審核或調查而向我們發出的任何指示。3.我們同意,本申請一旦獲批准,政府便可向市民公布以下資料:–本公司的名稱及聯絡資料;–本公司根據認可計劃獲認可為認證評核機構的資格;–本公司的認可範圍及該範圍的生效日期。表格第CAB-AA號(2006年版)-8-
簽署(獲授權代表):姓名:職位:電話:機構:日期:表格第CAB-AA號(2006年版)-8-